Mục lục
- I . Nguyên lý cơ bản
I . Nguyên lý cơ bản
Năm 1979, giải th−ởng Nobel về y học đã đ−ợc trao cho hai chuyên gia vật lý học là Cormack (Mỹ) và Hounsfield (Anh) vì những đóng góp của hai ông cho sự thành công của ph−ơng pháp chụp cắt lớp vi tính (CLVT). Sự kiện này nói lên những cống hiến to lớn của vật lý học cho y học đồng thời cũng thể hiện giá trị của ph−ơng pháp chụp CLVT trong chẩn đoán, điều trị và nghiên cứu khoa học y học.
Ngày 04/02/1991, chiếc máy chụp CLVT đầu tiên ở n−ớc ta đã bắt đầu hoạt động tại Bệnh viện Việt – Xô. Qua 15 năm, hiện đã có hơn 120 hệ thống chụp CLVT đ−ợc đ−a vào hoạt động trên toàn quốc, lợi ích của ph−ơng pháp chụp CLVT đã đ−ợc khẳng định trên thực tế lâm sàng ở n−ớc ta.
1. Lược sử
Radon (Đức) năm 1917 đã đặt cơ sở lý thuyết đầu tiên cho ph−ơng pháp toán học nhằm tái tạo cấu trúc của một vật thể 3 chiều trong không gian dựa trên vô số tận các hình chiếu của vật thể đó.
Bracewell (úc) năm 1956 lần đầu tiên áp dụng lý thuyết này trong quang phổ.
Cormack năm 1963 đã thành công trong việc tái tạo trên ảnh cấu trúc của một số vật thể hình học đơn giản nhờ một nguồn bức xạ của cô ban 60.
Hounsfield năm 1967 đã thiết kế đ−ợc một thiết bị dùng tia X để đo những vật thể thí nghiệm làm bằng các chất nhân tạo và lập đ−ợc ch−ơng trình máy tính để ghi nhớ và tổng hợp kết quả.
Ngày 1/10/1971 Hounsfield cùng Ambrose (Anh) cho ra đời chiếc máy chụp CLVT sọ não đầu tiên – Thời gian chụp và tính toán cho một quang ảnh lúc này cần 2 ngày.
Năm 1974 Ledley (Mỹ) hoàn thành chiếc máy chụp CLVT toàn thân đầu tiên “Whole body CT Scanner ACTA” – Thời gian chụp và tính toán cho một quang ảnh vài phút vẫn ch−a thuận tiện cho việc ứng dụng trong lâm sàng.
Cho tới năm 1977 mới có loại máy chụp CLVT với thời gian chụp một quang ảnh 20 sec trên thị tr−ờng thế giới, loại máy này còn mang tên máy chụp CLVT thế hệ 1. Hiện nay đã có máy chụp với thời gian d−ới 1 sec và máy siêu nhanh có thể chụp 0,1sec hoặc chụp xinê CLVT dùng trong chẩn đoán tim mạch.
2. Nguyên lý kỹ thuật
2. 1. Nguyên lý tạo ảnh
Chụp X quang cắt lớp qui −ớc dựa trên nguyên tắc là làm rõ các cấu trúc ở một mặt phẳng định tr−ớc và xoá đi hình chiếu của các mặt phẳng khác trên quang ảnh đó. Ph−ơng pháp này cho phép phân biệt sự chênh lệch tỷ trọng của các cấu trúc trên cùng một mặt phẳng cao nhất là 5%, hiện ít dùng vì liều xạ cao và độ phân giải ảnh thấp.
Dựa vào lý thuyết về tái tạo ảnh cấu trúc của một vật thể 3 chiều Hounsfield thiết kế một máy chụp CLVT gồm một hệ thống phát xạ QTX và những đầu dò (detector) đặt đối diện với bóng X.quang. Hệ thống này quay quanh một đường tròn tại một mặt phẳng vuông góc với trục cơ thể (hình 1a).
Chùm tia đi qua một cửa sổ hẹp (vài millimet) qua cơ thể bị hấp thụ một phần, phần còn lại sẽ đ−ợc đầu dò ghi lại. Kết quả ghi đ−ợc ở rất nhiều vị trí khác nhau của bóng X quang (cũng có nghĩa là nhiều hình chiếu của một lớp cắt cơ thể) sẽ đ−ợc chuyển vào bộ nhớ của một máy vi tính để phân tích. Ph−ơng pháp này cho phép phân biệt các cấu trúc cơ thể trên cùng một mặt phẳng có độ chênh lệch tỷ trọng 0,5%.
Hình 1b vẽ một vật thể hình vuông gồm 8×8 đơn vị thể tích. Nếu cho một nguồn QTX I0 chiếu qua từ 2 h−ớng, ta sẽ có kết quả thu đ−ợc ở 2 phía đối diện từ Ix1 đến Ix8 và Yy1 đến Yy8. Hai nhóm kết quả này không đủ để tính ra đ−ợc trị số hấp thụ QTX của từng đơn vị thể tích của vật thể nói trên. Muốn có 8×8 = 64 giá trị hấp thụ của 64 ô thể tích phải ghi đ−ợc 64 nhóm kết quả. Trong hệ thống máy chụp CLVT số lần đo quyết định số đơn vị thể tích của một lớp cắt và nh− vậy một lớp cắt càng chia ra nhiều đơn vị thể tích bao nhiêu thì ảnh của nó càng có độ phân giải không gian cao bấy nhiêu. Số đơn vị thể tích của một lớp cắt trong toán học gọi là ma trận (matrix). Máy chụp CLVT có nhiều loại ma trận: 256 x 256, 340 x 340, 512 x 512 và 1024 x 1024.
2.2. Kỹ thuật máy
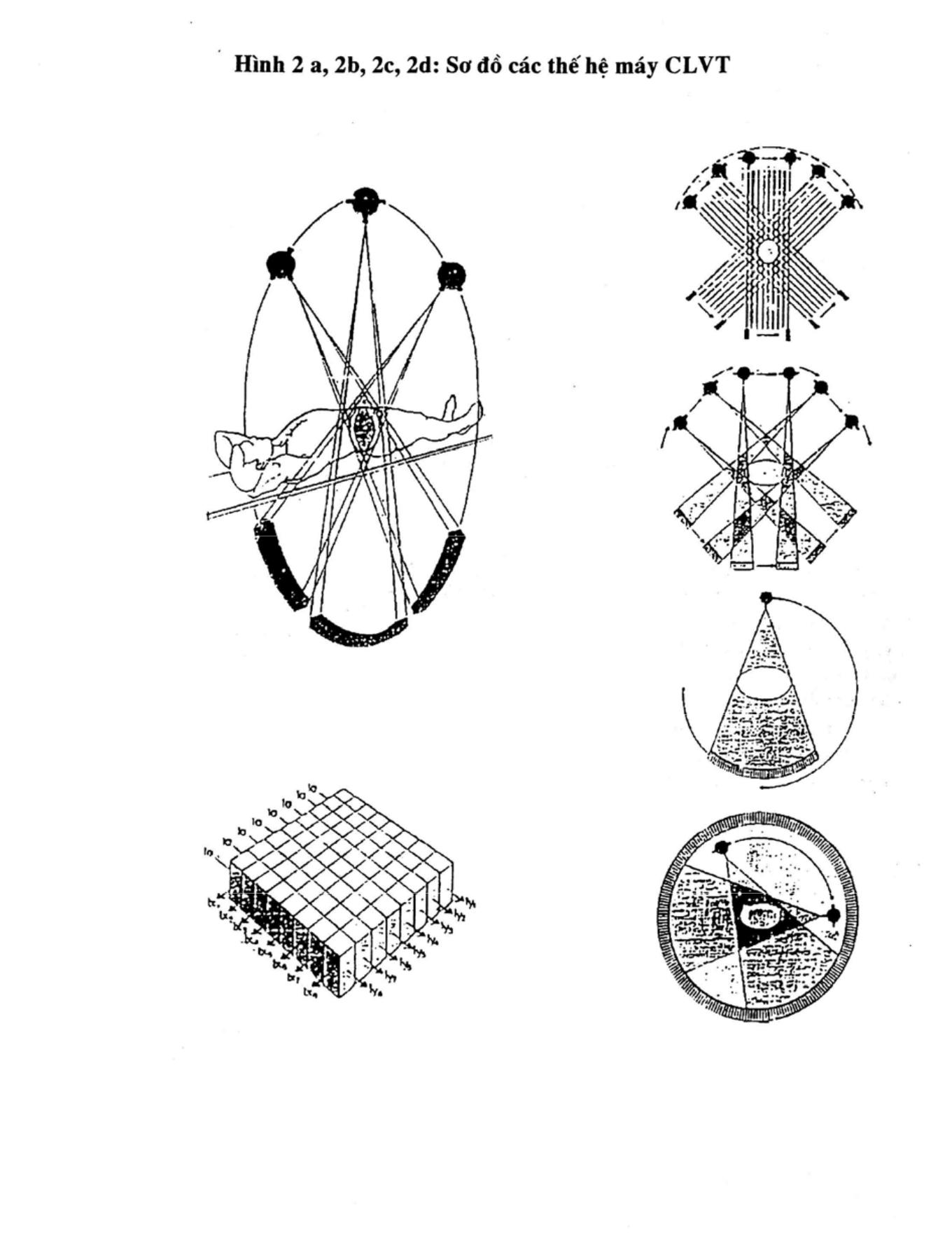
Về kỹ thuật cho đến nay đã hình thành 4 thế hệ máy dựa trên 4 nguyên tắc kỹ thuật về phát tia X và ghi kết quả khác nhau.
a. Thế hệ 1 (hình 2a)
Máy chụp có một đầu dò (detector), ứng dụng nguyên tắc quay và tịnh tiến. Chùm QTX d−ới 1o chiếu qua cơ thể tới 1 đầu dò để thu nhận kết quả. Bóng QTX phải quay quanh cơ thể 1800, khi quay đ−ợc 100 thì lại tịnh tiến một khoảng bằng chiều rộng cơ thể và phát tia để đo. Một quang ảnh phải mất vài phút.
b. Thế hệ 2 (hình 2b)
Máy chụp có nhiều đầu dò, quay + tịnh tiến:
Chùm QTX có góc mở rộng khoảng 100 đối diện với một nhóm từ 5 – 50 đầu dò. Máy cũng hoạt động theo nguyên tắc quay + tịnh tiến nh− trên nh−ng do chùm QTX rộng hơn nên giảm đ−ợc số lần quét ngang. Thời gian chụp 1 quang ảnh từ 6-20s.
c. Thế hệ 3 (hình 2c)
Máy chụp có nhiều đầu dò dùng nguyên tắc quay đơn thuần, chùm QTX có góc mở rộng hơn, trùm hết phần cơ thể cần chụp; 200 – 600 đầu dò ghép thành một cung đối diện với bóng X quang. Bóng QTX vừa quay vừa phát tia, dãy đầu dò quay cùng chiều với bóng và ghi lại kết quả. Thời gian chụp 1 quang ảnh từ 1- 4 s và độ dầy lớp cắt đạt tới 2mm.
d. Thế hệ 4 (hình 2d)
Máy chụp có hệ thống đầu dò tĩnh, gá cố định vào 3600 của đ−ờng tròn, số l−ợng đầu dò có thể lên đến vài ngàn bộ. Bóng QTX quay quanh trục cơ thể để phát tia. Thời gian chụp 1 quang ảnh có thể d−ới 1 sec rất thuận lợi cho khám xét các tạng có chuyển động.
2.3. Đơn vị thể tích, đơn vị ảnh, tỷ trọng
Một lớp cắt chia ra nhiều đơn vị thể tích – hình 1 thể hiện số đơn vị thể tích của nửa lớp cắt, trong đó a=b là cạnh vuông đáy của một đơn vị thể tích th−ờng từ 0,5 – 2mm, d là độ dày của lớp cắt đồng thời là chiều cao của đơn vị thể tích (từ 1mm đến 10mm). Mỗi đơn vị thể tích sẽ hiện lên ảnh nh− một điểm nhỏ, tổng các điểm hợp thành 1 quang ảnh (Volume element – Picture element). Độ hấp thụ tia X của từng đơn vị thể tích đ−ợc bộ nhớ ghi lại, cấu trúc hấp thụ càng nhiều tia X thì tỷ trọng càng cao, vì vậy ng−ời ta còn gọi ph−ơng pháp chụp CLVT là chụp cắt lớp đo tỷ trọng (Tomodensetometrie). Dựa vào kết quả đo độ suy giảm tuyến tính cuả chùm QTX, ng−ời ta tính ra tỷ trọng của cấu trúc theo đơn vị Hounsfield qua công thức:
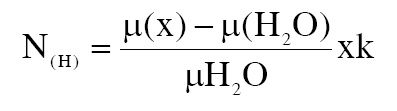
N( H ) : Trị số tỷ trọng tính bằng đơn vị Hounsfield của cấu trúc X
µ(x) : hệ số suy giảm tuyến tính của QTX khi xuyên qua đơn vị thể tích X.
H2O : Nước tinh khiết
k : Hệ số 1000 do Hounsfield đ−a ra và đã đ−ợc chấp nhận
Theo công thức trên, nếu X là:
– Nước (H2O) có trọng khối 1,000g/cm3 = 0 đơn vị H.
– Không khí có trọng khối 0.003g/cm3 = -1000 đơn vị H.
– Xương đặc có trọng khối 1.7000g/cm3 = +1700 đơn vị H.
2.4. Ảnh chụp CLVT, cửa sổ và bậc thang xám
Để phân tích đ−ợc những số đo của các cấu trúc cơ thể trên một lớp cắt cần biến chúng thành ảnh. Vì mắt th−ờng chỉ phân biệt đ−ợc d−ới 20 bậc thang xám từ đen đến trắng, nên ảnh chụp CLVT đặt 14-16 bậc xám khác nhau. Nh− vậy, ảnh CLVT không phải là ảnh trực tiếp của tia X lên phim mà là ảnh tạo lại từ bộ nhớ của máy tính vì vậy ph−ơng pháp chụp CLVT còn có tên gọi là chụp cắt lớp tái tạo ảnh (Tomographie par reconstruction) thấy sự chênh lệch tỷ trọng bên trong. Muốn nhìn toàn cục từ x−ơng đến phần mềm cần mở rộng cửa sổ. Điểm giữa của cửa sổ th−ờng đặt vào số đo trung bình của cấu trúc bình th−ờng mà ta cần khám xét; thí dụ não: 35, gan 50, phổi 700, x−ơng +200. Hình 4 vẽ sơ đồ mở cửa sổ trên giải Hounsfield và các số đo trung bình của một số cấu trúc trong cơ thể.
Mỗi ảnh chụp Hounsfield đều có ghi cửa sổ theo ký hiệu sau:
W (width): Độ rộng của cửa sổ
L (Level): Mức giữa của cửa sổ (có máy thay chữ L bằng chữ C: Center).
Sơ đồ cửa sổ trên dải đơn vị Hounsfield và hệ quả mảnh thể tích

2.5. Các yếu tố gây bất lợi cho ảnh
a. Hệ quả của mảnh thể tích (Partial volume effect)
Nh− đã nói trên ảnh chụp CL-VT là sự thể hiện số đo trung bình của các đơn vị thể tích qua bậc thang xám, vì vậy giới hạn của các vùng có tỷ trọng khác nhau sẽ không hoàn toàn trùng hợp với thực tế mà sẽ bị biến đổi một phần do giới hạn bị biến dạng theo các đơn vị thể tích (Hình 1). Hệ quả này đ−ợc khắc phục dần ở các thế hệ máy 3, 4 do số l−ợng của ma trận lớp cắt tăng lên cũng có nghĩa là đơn vị thể tích và đơn vị ảnh thu nhỏ lại.
b. Các nhiễu nhân tạo (artefact)
Những nguyên nhân sau đây có thể tạo nên những hình ảnh giả trên ảnh:
– Điện thế qua bóng QTX không thích hợp với độ dày cơ thể.
– Phần cơ thể cần chụp chuyển động trong lúc máy quét.
– Di vật kim loại hoặc chất cản quang trong cơ thể, trong quần áo bệnh nhân Những nhiễu nhân tạo trên ảnh sẽ làm cho ảnh không có giá trị chẩn đoán
3. Những tiến bộ của công nghệ chụp cắt lớp vi tính.
Từ thiết bị chụp cắt lớp vi tính đầu tiên đến nay, công nghệ chụp cắt lớp vi tính luôn luôn đổi mới nhằm vào hai mục tiêu chính là:
– Rút ngắn thời gian quét của bóng X quang cho một vòng quay 3600 quanh cơ thể ng−ời bệnh.
– Rút ngắn thời gian tạo ảnh và cải thiện chất l−ợng ảnh thông qua việc nâng cao độ phân giải đối quang thấp và độ phân giải không gian của ảnh.
3.1. Công nghệ chụp xoắn ốc
Là mốc quan trọng nhất về tiến bộ công nghệ chụp cắt lớp vi tính; công nghệ này bắt đầu đ−ợc ứng dụng trên lâm sàng từ năm 1991.
Trong chụp CLVT qui −ớc, cáp cao áp cấp điện cho bóng X quang cuộn một vòng khi bóng X quang quay một đ−ờng tròn 360o và sẽ phải quay ng−ợc chiều 360o để cáp điện cao áp không bị xoắn; lớp cắt tiếp theo đ−ợc thực hiện sau khi bóng dừng lại và quay ng−ợc chiều quay của lớp cắt tr−ớc . Thời gian nghỉ giữa hai lớp cắt khoảng trên 10 giây nên bệnh nhân không thể nhịn thở cho nhiều lớp cắt . Nhờ công nghệ tiếp điện qua vòng trựơt (slip ring) và bộ biến áp đặt ngay cạnh bóng Xquang trong khối quay nên bóng Xquang có thể quay liên tục cùng chiều, không cần thời gian nghỉ giữa hai lớp cắt . Bàn bệnh nhân đ−ợc tịnh tiến liên tục theo một h−ớng với tốc độ đều tạo nên hình quét của chùm QTX trên cơ thể là một đ−ờng xoắn liên tục không khép kín (hình 3a và 3b) .
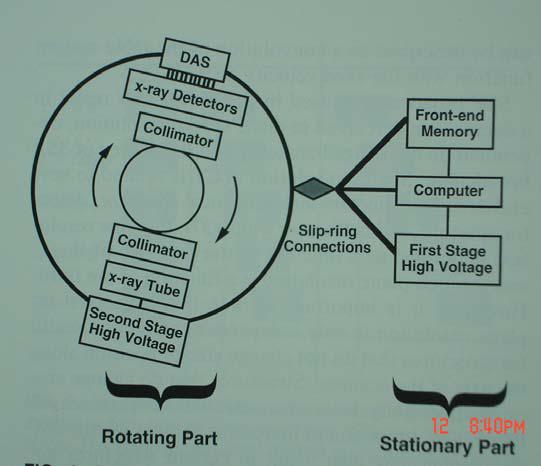
Hình 3a : Sơ đồ cấu trúc hệ thống chụp xoắn ốc
Phần quay gồm biến áp cao thế bậc II, bóng X quang, loa tụ quang, dãy đầu dò và bộ thu nhận dữ liệu DAS . Phần tĩnh gồm biến áp cao thế bậc I, máy tính và bộ nhớ
Công nghệ chụp xoắn ốc cho phép bóng X quang quay và phát tia X liên tục từ 10 đến 30, 60 giây và 90 giây. Nhờ vậy nếu một vòng quay của bóng cần 01 giây, ta có thể quét hộp sọ, lồng ngực hay ổ bụng mà chỉ cần bệnh nhân nhịn thở từ 20 đến 25 giây. Khám xét có thể thực hiện đ−ợc rất nhanh, nh−ng quan trọng hơn là:
– Dữ kiện thu được từ khám xét mang đặc điểm của thể tích một vùng cơ thể có tính liên tục, không phải là cộng dữ kiện của nhiều lớp cắt.
– Giảm được lượng thuốc cản quang tiêm vào cơ thể bệnh nhân mà chất lượng ảnh thu được lại có nồng độ thuốc cản quang trong mạch máu và tổ chức cao hơn.
– ảnh không gian 3 chiều (3D) dựng lại từ các dữ kiện có sẵn đạt đ−ợc chất lượng cao vì không bị khoảng phân cách giữa các lớp cắt, do đó ảnh chụp mạch máu, chụp x−ơng có giá trị chẩn đoán cao hơn.
Trong chụp CLVT xoắn ốc, một trị giá cần quan tâm là tỷ số của bàn (bệnh nhân)
chuyển động đối với một chu kỳ quay của bóng Xquang 360o gọi là Pitch :
Pitch = V(mm/s) x t (360o)/w
Pitch = độ dài chuyển động bàn BN trong một chu kỳ quay của bóng/ độ mở của chùm QTX (mm)
Thí dụ : Nếu bàn bệnh nhân tịnh tiến đ−ợc 5mm / một vòng quay 360o của bóng Xquang và độ mở chùm tia X rộng 5mm, ta có Pitch = 1.0 và thuật toán ngoại suy tuyến tính lúc này là 360 độ.
Nếu bàn bệnh nhân tịnh tiến đ−ợc 10mm/một vòng quay 360o của bóng trong khi độ mở chùm tia X vẫn là 5mm, ta có Pitch = 2.0 . Pitch = 2.0 đồng nghĩa với các vòng quét không còn liên tiếp nh− trong tr−ờng hợp Pitch = 1.0 nữa . Khi sử dụng Pitch >1.0, hầu hết các hệ thống chụp cắt lớp xoắn hiện nay đều tự động chuyển sang thuật toán ngoại suy 180o để giảm méo ảnh và chấp nhận tăng tỷ lệ nhiễu cũng nh− giảm độ phân giải đối quang .
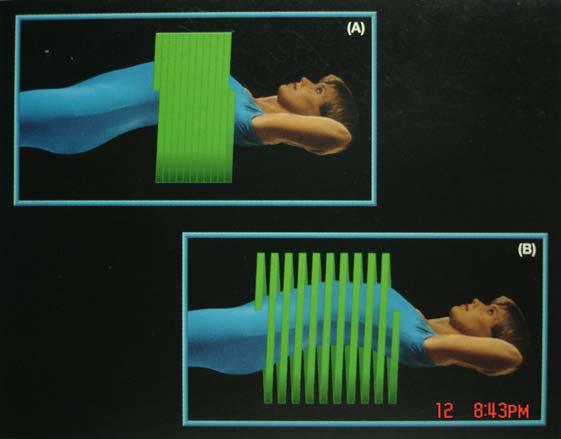
Hình 3b : Trong chụp xoắn ốc, Pitch thể hiện mức độ bao phủ của chùm tia
X trên phần cơ thể đ−ợc khám xét : (A) Pitch = 1:1 ; (B) Pitch = 2:1
3.2. Mốc tiến bộ thời sự hiện nay về chụp cắt lớp vi tính
Là công nghệ đa dãy đầu dò (Multidetector CT-Scanner theo tiếng Anh hoặc Scanner multibarettes theo tiếng Pháp). Loại máy này bắt đầu xuất hiện trên thị tr−ờng từ năm 1992 với hệ thống tạo đ−ợc 2 lớp cắt cho một vòng quay của bóng X quang (Twin hoặc Dual CT Scanner) . Năm 2001 đã có máy 4 lớp cắt cho một vòng quay 0,5 giây hay còn gọi là máy 8 lớp cắt/giây. Hiện nay, các hãng sản xuất đã nghiên cứu thành công loại máy 8, 16, 32 và 64 lớp cắt cho một vòng quay của bóng X quang với thời gian d−ới 0.5 giây. Công nghệ mới này cho phép chụp với độ dầy lớp cắt d−ới 1mm, nâng cao độ phân giải ảnh, khả năng tái tạo 3D và khả năng chẩn đoán của chụp cắt lớp vi tính lên rất nhiều, đặc biệt trong lĩnh vực chẩn đoán tim mạch .
Thí dụ với máy Dual (hai lớp cắt/vòng quay bóng Xquang), nếu đem so sánh với máy xoắn ốc đơn lớp, ng−òi sử dụng có thể đạt đ−ợc độ phân giải không gian dọc gấp đôi (5mmx2 thay cho 10mmx1) nếu giữ nguyên tốc độ tịnh tiến bàn bệnh nhân, thể tích khám xét và c−ờng độ dòng điện qua bóng . Nếu giữ nguyên độ phân giải không gian dọc, thể tích khám xét và dòng qua bóng, máy Dual giảm đ−ợc 50% thời gian quét (15giây thay cho 30giây) . Nếu giữ nguyên độ phân giải, tốc độ bàn bệnh nhân và dòng qua bóng, máy Dual cho phép khám xét một thể tích gấp đôi (60cm thay cho 30cm) .

Hình 4 : So sánh máy đơn lớp và máy hai lớp cắt : Giữ nguyên mA, tốc độ chuyển bàn và thể tích vùng khám xét, máy hai lớp giảm 1/2 độ dầy lớp cắt và do đó tăng gấp đôi độ phân giải dọc
3.3. Chiếu X quang cắt lớp vi tính
Cũng là công nghệ mới xuất hiện từ năm 1997. Do yêu cầu thực hiện các chọc dò sinh thiết ở vùng sâu trong cơ thể, nhất là ở những khu vực mà siêu âm gặp khó khăn (thí dụ phổi, x−ơng); một số hãng sản xuất đã tạo đ−ợc công nghệ chiếu cắt lớp vi tính với 6 đến 8 ảnh/giây và l−ợng mA thấp (10-30mA). Công nghệ mới này cho phép làm sinh thiết d−ới h−ớng dẫn của cắt lớp vi tính với độ chính xác cao.
4. Ứng dụng chụp cắt lớp vi tính trong lâm sàng
4.1. Chụp CLVT không dùng thuốc cản quang
Hầu hết các khám xét CL-VT đều bắt đầu bằng chụp không có thuốc cản quang. Dựa vào các dấu hiệu lâm sàng, X quang và siêu âm… để chọn vùng đ−a vào chụp cắt lớp. Mọi khám xét CLVT đều cắt lớp vuông góc với trục chính cơ thể thể trừ sọ não có thể cắt theo mặt phẳng đứng ngang nếu cần thiết. Độ dày của lớp cắt th−ờng dùng 8 – 10mm với b−ớc chuyển bệnh nhân 8-10mm. Đối với nền sọ, hố yên, x−ơng đá, th−ợng thận phải dùng lớp cắt mỏng hơn: 2 hoặc 5mm. Có thể dùng b−ớc chuyển nhỏ hơn độ dày của lớp cắt để không bỏ lọt bất th−ờng ở nơi tiếp giáp giữa hai lớp.
Tái hiện ảnh ở những mặt phẳng khác (Reformating). Sau khi đã có dữ kiện của những lớp cắt trong bộ nhớ, ta có thể dựng lại ảnh theo những mặt phẳng do thầy thuốc tự chọn thí dụ đứng dọc, đứng ngang, chếch…
Hiện ảnh theo không gian 3 chiều: Những máy sản xuất từ thập kỷ 90 thường có ghép chương trình này. Có thể yêu cầu máy cho ảnh 3 chiều với những khoảng mở tự chọn (Tridimensional dissplay), các ảnh này đặc biệt quý cho các phẫu thuật viên sọ não.
a. Đánh giá cấu trúc trên các lớp cắt th−ờng là gọi ra số đo trung bình theo tỷ trọng Hounsfield để nhận xét. Dựa vào số đo trung bình của mô lành, ta có 3 loại cấu trúc dựa theo tỷ trọng:
– Tăng tỷ trọng hoặc tăng đậm độ (Hyperdense): Vùng cần đo có số đo cao hơn mô lành của cùng cá nhân đó.
– Giảm tỷ trọng hoặc giảm đậm độ (Hypodense): kết quả thấp hơn mô lành của cùng tạng, cùng ng−ời.
– Cùng tỷ trọng hoặc cùng đậm độ (isodense): kết quả ghi đ−ợc t−ơng tự nh− mô lành của tạng đó trên cùng ng−ời đó.
Đối với các ổ bất th−ờng tăng hoặc giảm tỷ trọng, nếu nắm vững cơ thể học cắt lớp ngang ta có thể nhận biết không khó khăn nh−ng việc nhận biết các ổ bất th−ờng đồng đậm độ nhiều khi rất phức tạp: phải dựa vào các dấu hiệu gián tiếp và nhờ sự trợ giúp của thuốc cản quang.
b. Những biến đổi chính về bệnh học hình thái:
Các cấu trúc trong cơ thể sống không thể xem xét nh− một vật thể tĩnh đ−ợc. Chúng phản ứng lại với các tác nhân nh− chấn th−ơng, nhiễm trùng, sinh u và biến đổi chuyển hoá bằng những cách khác nhau. Những biến đổi này có thể thấy đ−ợc một phần trên ảnh chụp CLVT.
– Dịch trong kén, dịch viêm, dịch thấm
Trong cơ thể có thể gặp kén ở nhiều tạng. Dịch trong khoang kín của kén có tỷ trọng gần với n−ớc (H2O). Tỷ trọng này phụ thuộc nhiều nhất vào l−ợng protein trong dịch. Dịch kén là một khoang vô mạch nên tỷ trọng sẽ không đổi nếu ta đ−a thuốc cản quang vào mạch máu.
Dịch tiết hay dịch viêm có l−ợng protein trên 30g/lít có thể đạt tỷ trọng 20-30 đơn vị H.
Dịch thấm ít protein hơn, tỷ trọng gần với n−ớc.
– Máu – ổ máu tụ
Tỷ trọng của máu phụ thuộc nhiều nhất vào l−ợng protein của các phần tử hữu hình, nếu lấy hết các phần tử hữu hình đi, tỷ trọng của máu sẽ giảm từ 55 đơn vị xuống 15-20 đơn vị H.
Máu cục trong ổ máu tụ có tỷ trọng cao hơn hẳn máu tuần hoàn. Quá trình tiêu ổ máu tụ, tiêu sợi huyết và các phần tử hữu hình cũng nh− hiện t−ợng cơ thể hấp thụ lại Anbumin của
ổ máu tụ làm cho tỷ trọng máu tụ giảm dần; hiện t−ợng tăng tỷ trọng tồn tại từ 1 đến 2 tuần sau chảy máu tuỳ theo khối l−ợng của ổ máu tụ. Sau đó tỷ trọng trở nên cân bằng với tổ chức hạt (phần mềm) và sau hơn 2 tuần tỷ trọng có thể thấp hơn mô mềm. Tại các ổ máu tụ lớn có thể hình thành một bao do tổ chức tạo thành. Tỷ trọng giảm dần theo sự giảm Anbumin trong bao và cuối cùng ta có thể có một kén dịch.
Giai đoạn tăng tỷ trọng của ổ máu tụ rất quý trong chẩn đoán vì nó rất đặc hiệu. Bỏ qua tuần lễ đầu, chẩn đoán sẽ khó khăn hơn nhiều vì phải loại trừ những quá trình khác có tỷ trọng t−ơng tự.
– áp xe hoá
Quá trình viêm không hồi phục dẫn đến sự hình thành ổ áp xe. Tổ chức hoại tử, dịch viêm và các bạch cầu chết là thành phần chính của mủ. Tr−ờng hợp điều trị tốt, một ổ áp xe sẽ tự tiêu và trên ảnh chụp CLVT sẽ thấy một kén mà dịch kén giàu Anbumin. Thông th−ờng mủ có tỷ trọng 30 đơn vị H. Tổ chức hạt bao quanh áp xe rất giàu tuần hoàn nên khi đ−a thuốc cản quang vào tĩnh mạch ta sẽ có một bao tăng tỷ trọng bọc quanh ổ áp xe, thể hiện trường
hợp của một áp xe mới hoàn chỉnh. Các ổ áp xe mãn tính có vỏ hiện rõ trên ảnh chụp CLVT không tiêm thuốc cản quang. Tỷ trọng mủ chứa trong áp xe theo thời gian có thể giảm xuống gần với n−ớc.
– Những biến đổi khác
Hiện tượng vôi hoá ổ hoại tử hoặc vôi hoá protein rất th−ờng gặp trên phim X quang cho thấy một tỷ trọng rất cao trên ảnh chụp CLVT: tuỳ theo mức độ thấm vôi, tỷ trọng của ổ bệnh xuất hiện cao hơn ổ máu tụ cho đến tỷ trọng của x−ơng cứng.
Thoái hoá kính và thoái hoá bột chứa Anbumin trong tế bào hoặc trong tổ chức kẽ không cho thấy sự thay đổi tỷ trọng.
Các ổ hoại tử trái lại thể hiện giảm tỷ trọng rõ rệt trong quá trình dịch hoá tổ chức. Ta gặp các ổ này trong viêm không hồi phục và trong các u phát triển nhanh do thiếu oxy tổ chức hoặc chảy máu trong u.
4.2. Chụp CLVT có áp dụng chất cản quang
Hai hình thức chính đ−a thuốc cản quang vào cơ thể là:
Đưa vào khoang tự nhiên và đưa vào lòng mạch.
a. Đưa thuốc cản quang vào khoang tự nhiên.
Các khoang tự nhiên như ống tiêu hoá, các tạng rỗng hay chứa dịch, khoang dịch não tuỷ đều có thể đưa cản quang vào để làm rõ hơn hình dáng, đ−ờng bờ, các thành phần chứa bên trong và mối liên quan với các cấu trúc lân cận.
Khác với việc áp dụng thuốc cản quang trong X quang quy −ớc, chất cản quang dùng trong chụp CLVT cần có những tiêu chuẩn sau:
– Dung dịch phải có độ cản quang ổn định: chất cản quang phải đ−ợc hoà tan trong dịch, không có hiện tượng lắng, kết tủa…
– Dung dịch cản quang cần có áp lực thẩm thấu cân bằng với cơ thể (330 mosmol/kg) để tránh hiện tượng cô đặc hoặc hoà loãng thuốc cản quang do trao đổi dịch với cơ thể.
– Độ cản quang của dung dịch không đ−ợc cao quá để tránh các nhiễu nhân tạo trên ảnh giống như trường hợp kim loại trong cơ thể. Độ cản quang thích hợp của dung dịch là 150
– 200 đơn vị H.
b. Đ−a thuốc cản quang vào lòng mạch.
– Hình thức chủ yếu là tiêm vào tĩnh mạch loại thuốc cản quang thải trừ qua đ−ờng thận. Dựa vào những hiểu biết về d−ợc động học của thuốc cản quang trong cơ thể để quyết định l−ợng thuốc, tốc độ bơm và thời điểm chụp CLVT so với thời điểm bơm thuốc (chi tiết xin xem phần II) .
4.3. Lượng nhiễm xạ trong chụp CLVT
Liều nhiễm xạ tại vùng cơ thể chụp CLVT t−ơng đ−ơng với liều tại chỗ của một lần khám đại tràng hoặc chụp thận tiêm tĩnh mạch (2-3 rad) . Các thế hệ chụp xoắn ốc hiện có thêm bộ phận điều chỉnh mA tự động theo độ dầy của vùng khám xét kết hợp hệ thống đầu dò chất rắn có độ nhậy cao nên giảm đ−ợc liều xạ so với những máy sản xuất cũ .
Liều sinh dục: do cấu trúc của máy bảo vệ tốt nên th−ờng thấp hơn nhiều so với khám X quang qui −ớc nếu không chụp CLVT trực tiếp tại vùng có cơ quan sinh dục.
4.4. Chỉ định chụp cắt lớp vi tính trong lâm sàng
Ưu thế của chụp cắt lớp vi tính trong phát hiện các cấu trúc bất th−ờng so với X quang qui −ớc là nhờ độ phân giải đối quang thấp; nếu sự khác biệt về đậm độ cấu trúc trong cơ thể có thể thấy đ−ợc trên X quang chuẩn là 5% thì chụp cắt lớp vi tính cho phép phát hiện sự khác biệt tỷ trọng tới mức 0,5%.
Nhờ chụp cắt lớp vi tính cho phép đo tỷ trọng của các cấu trúc trong cơ thể, có thể dự đoán cấu trúc bất th−ờng đó là mỡ, dịch, mô mềm, máu tụ hay thấm vôi, không khí. Hiện nay chụp cắt lớp vi tính có chỉ định rất rộng, d−ới đây là những chỉ định chính trong lâm sàng.
a. Sọ não
Các cấu trúc bên trong hộp sọ, X quang qui −ớc, X quang mạch máu và điện não đồ th−ờng không đủ để thăm dò, nhất là về hình thái. Chụp cắt lớp vi tính sọ não, do đó là chỉ định hay dùng nhất đối với các bệnh lý nội sọ.
– Chấn thương sọ não
Các ổ máu tụ ngoài màng cứng do chấn th−ơng có vỡ x−ơng th−ờng không khó khăn trong chẩn đoán lâm sàng. Đặc biệt có ích trong các ổ máu tụ nội não, các ổ máu tụ d−ới màng cứng, nhất là các ổ máu tụ mãn tính, không có vỡ x−ơng sọ. Các ổ máu mãn tính th−ờng có tỷ trọng bằng hoặc thấp hơn tổ chức não, đôi khi phải áp dụng thuốc cản quang tĩnh mạch để làm hiện rõ chúng. Các ổ máu tụ đồng thời cả hai phía đối diện của hộp sọ, hoặc ở những vùng không gây chuyển dịch vị trí của động mạch não th−ờng không thể phát hiện đ−ợc chụp động mạch.
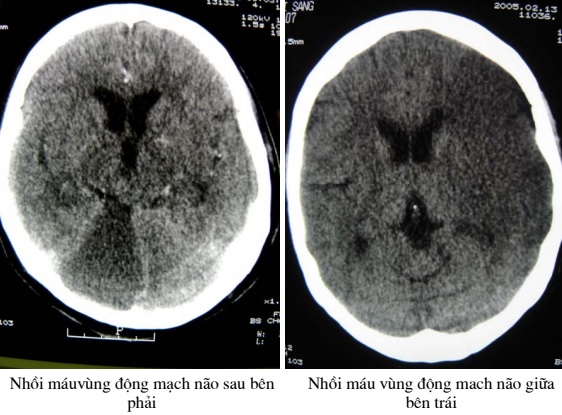
– Các tai biến mạch máu não
Trên ảnh cắt lớp vi tính có thể dễ dàng phân biệt ổ máu tụ do chảy máu với những ổ giảm tỷ trọng do nhồi máu hoặc tắc mạch não. Phát hiện tắc mạch não gây nhồi máu trên ảnh chụp cắt lớp vi tính th−ờng đạt đ−ợc sau đột quỵ từ 12 đến 24 giờ. Chụp cắt lớp đặc biệt có ích cho điều trị phẫu thuật sớm các tr−ờng hợp chảy máu – tụ máu.
– Các tổn thương do viêm
Nói chung các tổn th−ơng viêm não lan toả th−ờng khó phát hiện trên ảnh cắt lớp vi tính. Các
ổ viêm khu trú hoặc di chứng của viêm não nhiều ổ khu trú cho thấy những ổ giảm tỷ trọng não.
Bệnh viêm não tủy – chất trắng cũng cho thấy những hình ảnh có thể phân biệt với viêm não lan toả. Các ổ áp xe não do nhiễm trùng dễ dàng phát hiện bằng chụp cắt lớp vi tính nhất là đối với áp xe mãn tính. Tiêm thuốc cản quang vào tĩnh mạch kết hợp chụp cắt lớp vi tính có thể làm hiện rõ bao của ổ áp xe .
Các tổn th−ơng khu trú thành ổ trong não do ký sinh trùng cũng là một chỉ định của chụp cắt lớp vi tính.
– U não
Chụp cắt lớp vi tính cho phép xác định vị trí, độ lớn và dự đoán cấu trúc của u. Để dự đoán bản chất của u th−ờng phải tiêm cản quang tĩnh mạch để đánh giá l−ới tuần hoàn trong u. Tuy vậy việc phân biệt một u não, áp xe não và nhồi máu bao giờ cũng phải kết hợp với bệnh cảnh lâm sàng.
Chụp cắt lớp vi tính còn giúp phát hiện những dị tật bẩm sinh của các cấu trúc bên trong sọ.
b. Chụp cắt lớp vi tính toàn thân
Có 2 loại chỉ định khám cắt lớp vi tính chính:
– Khám để phát hiện, chẩn đoán và chẩn đoán phân biệt. Đó là những tr−ờng hợp mà các ph−ơng pháp thăm dò khác nh− X quang qui −ớc, xét nghiệm sinh hoá – huyết học, siêu âm….
không đ−a lại đ−ợc chẩn đoán d−ơng tính. Nói chung các thăm dò khác th−ờng đi tr−ớc chụp cắt lớp vi tính.
– Chụp để đánh giá sự lan rộng của ổ bệnh nhằm xác lập ph−ơng pháp điều trị thích hợp nhất, an toàn và tiết kiệm cho bệnh nhân.
Đối với các nhân phổi kích th−ớc từ 3 – 10mm, X quang và cắt lớp qui −ớc chỉ có thể phát hiện từ 20 – 40%, chụp cắt lớp vi tính cho phép phát hiện đ−ợc 80% các nhân phổi. Đối với phẫu thuật bụng và ngực, chụp cắt lớp vi tính còn giúp cho phẫu thuật viên giảm đ−ợc đáng kể những bất ngờ trong mổ và lập đ−ợc ch−ơng trình mổ thuận lợi vì nó cho thấy đ−ợc mối liên quan của ổ bệnh với các tạng lân cận, phân bậc TNM tổn th−ơng.
c. Bảng ghi tóm tắt các chỉ định chụp cắt lớp vi tính toàn thân:
|
Tên cơ quan và loại bệnh |
Khám xét |
||
|
đi trước |
|||
|
Hố mắt: |
U |
X quang |
|
|
Viêm giả U, viêm |
|||
|
Chấn th−ơng |
|||
|
Mặt và nền sọ: |
U |
X quang |
|
|
Viêm |
|||
|
Cổ: |
U |
X quang |
|
|
áp xe thành họng |
|||
|
Trung thất: |
U nguyên phát |
X quang |
|
|
U thứ phát |
|||
|
Viêm trung thất |
|||
|
Bệnh lý động mạch chủ ngực |
|||
|
Hạch trung thất và rốn phổi |
|||
|
Phổi: |
U nguyên phát |
X quang |
|
|
Di căn |
|||
|
Lao phổi |
|||
|
Giãn phế quản |
|||
|
Giãn phế nang |
|||
|
Tim: |
Bất th−ờng cơ tim và màng ngoài tim |
X quang |
|
|
Gan: |
Chấn th−ơng |
Siêu âm |
|
|
U nguyên phát và thứ phát |
|||
|
áp xe |
|||
|
Thoái hoá mỡ |
|||
|
Đ−ờng mật: túi mật: |
Chẩn đoán vị trí và nguyên tắc mật, u đ−ờng mật |
Siêu âm |
|
|
Tuỵ tạng: |
U |
Siêu âm |
|
|
Viêm cấp, viêm mạn |
|||
|
áp xe tuỵ |
|||
|
Giả kén tuỵ |
||
|
Thận và khoang quanh thận: U, kén |
Siêu âm |
|
|
Teo, kém phát triển |
||
|
Thận ứ n−ớc |
||
|
Sỏi thận – niệu quản |
||
|
Chấn th−ơng |
||
|
Viêm, apxe, lao |
||
|
Tuyến th−ợng thận: |
U tuyến |
Siêu âm |
|
Quá sản tuyến |
||
|
Tử cung – buồng trứng: |
Các khối u |
Siêu âm |
|
Bàng quang, tuyến tiền liệt: |
Khối u |
Siêu âm |
|
Phì đại lành tính |
||
|
Khoang phúc mạc: |
U các tạng trong khoang phúc mạc |
Siêu âm |
|
Apxe |
||
|
Cột sống: |
Chấn th−ơng |
X quang |
|
Thoát vị đĩa dệm |
||
|
Lao, u cột sống |
||
|
Cơ x−ơng khớp: |
U nguyên phát và thứ phát |
X quang |
|
Chấn th−ơng |
||
|
Cấu trúc |
Tên hoạt chất |
Độ nhớt ở 37oC |
Áp lực thẩm thấu |
Tên thương phẩm |
|
* |
( 300mg iode/ml) |
|||
|
Ionic |
Iothalamate |
3 |
1500-1600 |
Conray |
|
monome |
Vasoray |
|||
|
Metrizoate |
Isopaque |
|||
|
Amidotrizoate |
Urografin |
|||
|
Angiografin |
||||
|
Gastrografin |
||||
|
Ioxithalamate |
Telebrix |
|||
|
Ionic dime |
Ioxaglate |
6 |
600 |
Hexabrix |
|
Non-ionic |
Iohexol |
6 |
500-700 |
Omnipaque |
|
monome |
Iopamidol |
Iopamiro |
||
|
Iopromide |
Ultravist |
|||
|
Ioversol |
Optiray |
|||
|
Iobitridol |
Xenetix |
|||
|
Non-ionic |
Iodixanol |
10 |
300 |
Visipaque |
|
dime |
Iotrolan |
Isovist |
Độ nhớt tính theo đơn vị cP độ thẩm thấu tính theo mOsm/kg H2O
Độc tính của chất đối quang iode có thể là tổng hợp của 3 yếu tố : độc tính hoá học của các phân tử chất đối quang, độc tính do áp lực thẩm thấu cao của dung dịch và độc tính do gây mất cân bằng ion . Do đó, nên chọn các dung dịch đối quang iode tiêm có độ thẩm thấu thấp, gần với độ thẩm thấu của cơ thể và chất đối quang dạng không ion khi sử dụng cho bệnh nhân có nguy cơ cao bị tác dụng không mong muốn .
Tác dụng không mong muốn (ADR) : Các chất đối quang iode dạng ion và không ion đều có thể gây ADR khi tiêm vào mạch máu . Tần xuất chung ADR của các chất đối quang iode dạng ion dùng qua đ−ờng tiêm vào mạch máu khoảng trên 3% . Theo một báo cáo của uỷ ban an toàn về sử dụng chất đối quang Nhật bản với số l−ợng bệnh nhân trên 160.000 cho mỗi nhóm (có ion và không ion) thì tần xuất ADR giảm đ−ợc 3/4 nếu dùng chất đối quang không ion . Có thể xếp ADR theo 5 nhóm :
1. Phản ứng tăng nhậy cảm cho đến choáng dạng phản vệ
2. Phản ứng tim mạch
3. Suy chức năng thận
4. Rối loạn đông máu và tổn th−ơng nội mạc mạch máu
5. Phản ứng của hệ thần kinh trung −ơng và đôi khi kèm theo mù một hoặc cả hai mắt Về mức độ phản ứng, có thể phân loại nhẹ (th−ờng gặp), vừa (ít gặp) và nặng (hiếm gặp)
Nhẹ : cảm giác nóng theo đ−ờng tĩnh mạch từ vị trí tiêm lan lên cổ và mặt, ngứa, nổi mề đay, buồn nôn, nôn, rối loạn vị giác, hắt hơi, lo âu . Ho và khó thở . Đau dọc theo tĩnh mạch tiêm . Vừa : các dấu hiệu kể trên ở mức cao hơn, đặc biệt là nổi mề đay, nôn, khó thở và lo sợ . Co thắt phế quản làm tăng thêm khó thở, hạ huyết áp . Mức phản ứng này gặp khoảng 0,5-1% các tr−ờng hợp tiêm chất đối quang iode .
Nặng : Các dấu hiệu mô tả trên ở mức rất cao, đặc biệt là khó thở, co thắt phế quản, tụt huyết áp, co giật toàn thể . Rối loạn ý thức, phù thanh môn . Truỵ tim mạch có thể xảy ra cùng với phù phổi; loạn nhịp tim dẫn đến ngừng tim . Tỷ lệ gặp phản ứng nặng khoảng 0,2% các tr−ờng hợp tiêm thuốc đối quang iode .
Tử vong : Một số rất ít bệnh nhân có thể bị tử vong dù đã cấp cứu tích cực và kịp thời . Nguyên nhân tử vong hay gặp là suy hô hấp và tuần hoàn nặng, phù phổi cấp và tắc đ−ờng thở do co thắt phế quản nặng . Một vài tr−ờng hợp tử vong kiểu choáng tim còn gặp rất sớm sau tiêm chất đối quang mà không có triệu chứng báo trứơc . Ch−a có tỷ lệ tử vong chính xác nh−ng hồi cứu đa trung tâm với số l−ợng bệnh nhân lớn cho thấy hai nhóm kết quả : nhóm 1 từ 1:15.000 -1:17.000 và nhóm 2 từ 1: 40.000 đến 1: 80.000 .
Các thuốc cản quang th−ờng dùng trong chụp cắt lớp vi tính là :
+ Các thuốc cản quang đơn phân tử có ion: -Radiosélectan 60%: 300mgI/ml
– Radiosélectan 76%: 380mgI/ml
-Télébrix 35 và 38: 350 và 380mgI/ml
Các thuốc cản quang trên có áp lực thẩm thấu cao hơn áp lực thẩm thấu của huyết tương tới 5-6 lần
+Thuốc cản quang có ion chứa hai phân tử gắn 6 nguyên tử iod Hexabrix 320: 320mgI/ml
+ Thuốc cản không ion: có các gốc dài hơn và có độ ái n−ớc cao hơn. –
- Ultravist 300 : 300mgI/1ml
- Iopamiron 370: 370mgI/ml
- Iopamiron 300: 300mgI/ml
- Pamiray (có cùng gốc hoá học với Iopamiron) – Xenetix 300 : 300mgI/ml
- Omni paque 300: 300mgI/ml
- Optiray 300: 300mgI/ml
Các thuốc này có áp lực thẩm thấu chỉ cao hơn áp lực thẩm thấu của huyết t−ơng rất ít,
chúng đ−ợc sử dụng rộng rãi trong x quang tiết niệu, x quang mạch máu và chụp cắt lớp vi
15
tính , một số có thể bơm vào khoang d−ới nhện tuỷ sống và các khoang khác của cơ thể theo hàm l−ợng thích hợp .
2. Đề phòng các tai biến liên quan đến thuốc cản quang:
– Các yếu tố nguy cơ: bệnh tim, mắc bệnh mạch máu, suy thận, đái đ−ờng, mất n−ớc, tiêm thuốc cản quang các lần quá gần nhau, cơ địa dị ứng, ng−ời có chứng luôn lo lắng…
– Dùng các thuốc dự phòng: nhất thiết phải dùng thuốc dự phòng cho một số tr−ờng hợp nhất định ( cơ địa dị ứng, đã có phản ứng với thuốc cản quang…), các tr−ờng hợp có nguy cơ phản ứng thuốc .
– Các cách dùng thuốc dự phòng:
.Atarax100mg: 1 viên /ngày trong 3 ngày tr−ớc khi làm thủ thuật
. Tiêm 2 ống solumédrol 40mg tr−ớc khi tiêm thuốc cản quang .
.Dùng thuốc cản quang có áp lực thẩm thấu thấp
.Tôn trọng liều dùng thuốc cản quang
.Khi có nguy cơ về thận, cần đảm bảo cơ thể không thiếu n−ớc
.Trong mọi tr−ờng hợp cần theo dõi sát bệnh nhân và luôn giữ đ−ờng tĩnh mạch.
3. Chuẩn bị bệnh nhân khi dùng thuốc cản quang tĩnh mạch
• Hỏi kỹ tiền sử dị ứng với thuốc, thời tiết, thức ăn, hen phế quản
• Khám xét loại trừ suy thận, suy tim mất bù
• Trừ cấp cứu, bệnh nhân phải nhịn đói tr−ớc 6giờ
• Không cần làm test vì không có giá trị dự phòng
• Đặt đ−ờng truyền tĩnh mạch và l−u kim ít nhất 15phút sau tiêm
4. Các biểu hiện lâm sàng của ADR và cách xử trí
4.1- Biểu hiện nhẹ:
-Biểu hiện nhẹ th−ờng luôn kèm với các bệnh nhân quá lo âu, nên luôn phải giải thích rõ để bệnh nhân yên tâm và hợp tác khi làm thủ thuật.
-Có thể có các biểu hiện ở đ−ờng hô hấp( ho, tức thở), biểu hiện ở đ−ờng tiêu hoá( nôn và buồn nôn), biểu hiện thần kinh( hoảng sợ, đau đầu). Các biểu hiện này có thể đơn độc hay phối hợp
+Xử trí: cho bệnh nhân hít thở mạnh vài lần để tránh căng thẳng cũng có thể làm mất các triệu chứng, có thể phải chuẩn bị 1g hydrocortison pha dịch truyền để truyền cho bệnh nhân khi không đỡ.
4.2 – Các biểu hiện nặng, sốc phản vệ
(theo thông t− h−ớng dẫn của Bộ y tế số 08/1999-TT-BYT ngày 04/5/99)
• Triệu chứng :
– Cảm giác khác th−ờng nh− bồn chồn, lo âu, hoảng sợ
– Mẩn ngứa, ban đỏ, mày đay, phù Quincke
– Mạch nhanh nhỏ, tụt huyết áp có khi không đo đ−ợc
– Khó thở, nghẹt thở (kiểu hen, phù thanh quản)
– Đau quặn bụng, ỉa đái không tự chủ
– Đau đầu, chóng mặt , đôi khi mất ý thức
– Choáng váng, vật vã, giãy giụa, co giật
• Xử trí
A- Xử trí ngay tại chỗ
– Ngừng ngay thuốc cản quang đang tiêm
– Đặt bệnh nhân nằm tại chỗ, đầu thấp, chân cao và ủ ấm cho bệnh nhân, nằm nghiêng nếu có nôn .
– Thuốc : Adrenalin là thuốc cơ bản để chống sốc phản vệ :
Adrenaline dung dịch 1/1.000 (ống 1ml =1mg) tiêm d−ới da ngay sau khi xuất hiện triệu chứng với liều nh− sau :
+ 1/2 – 1ống cho ng−ời lớn
+ Trẻ em : hoà loãng 1 ống 1ml với 9ml n−ớc cất rồi tiêm 0,1ml/kg cân nặng của trẻ .
16
+ Tiếp tục Adrenaline liều nh− trên 10-15phút một lần cho tới khi huyết áp trở lại bình th−ờng .
+ Nếu sốc quá nặng đe doạ tử vong, có thể pha loãng 1 ống 1ml với 9ml n−ớc cất và tiêm tĩnh mạch .
B- Tuỳ theo điều kiện trang thiết bị y tế và trình độ chuyên môn của từng tuyến có thể áp dụng các biện pháp sau :
– Xử trí suy hô hấp
Tuỳ mức độ khó thở có thể sử dụng các biện pháp sau :
+ Thở Oxy đ−ờng mũi – thổi ngạt
+ Bóp bóng Ambu có oxy
+ Đạt ống nội khí quản, thông khí nhân tạo . Mở khí quản nếu phù thanh môn
+ Truyền tĩnh mạch chậm Aminophylline 1mg/kg/giờ hoặc terbutaline 0,2microgam/kg/phút .
+ Có thể dùng Terbutaline 0,5mg 1ống d−ới da ở ng−ời lớn và 0,2mg/10kg cơ thể ở trẻ em
. Tiêm nhắc lại nếu sau 6-8giờ không đỡ khó thở .
+ Xịt họng terbutaline/sabutamol .
– Duy trì huyết áp :
Truyền tĩnh mạch adrenaline để duy trì huyết áp : 0,1microgam/kg/phút, điều chỉnh tốc độ truyền theo huyết áp, tối đa 2mg adrenaline/giờ cho ng−ời lớn 55kg .
– Các thuốc khác
+ Methylprednisolon 1-2mg/kg/4giờ hoặc hydrocortisone hemisuccinate 5mg/kg/giờ tiêm tĩnh mạch ( có thể tiêm bắp ở tuyến cơ sở) . Dùng liều cao gấp 2-5 lần nếu sốc nặng
+ Natriclorua 0.9% 1-2lít ở ng−ời lớn, không quá 20ml/kg ở trẻ em .
+ Diphenhydramin 1-2mg tiêm bắp hay tĩnh mạch
Chú ý
– Theo dõi bệnh nhân ít nhất 24 giờ sau khi huyết áp đã ổn định
– Nếu không lấy đ−ợc tĩnh mạch ở khuỷu tay, cẳng tay nên tận dụng đ−ờng tĩnh mạch đùi .
– Có thể truyền thêm huyết t−ơng, albumin hoặc dung dịch cao phân tử nếu các biện pháp trên không nâng đ−ợc huyết áp .
– Điều d−ỡng/kỹ thuật viên có thể sử dụng adrenaline 1ống1mg d−ới da nếu bác sĩ ch−a kịp có mặt
– Chuẩn bị sẵn sàng hộp thuốc cấp cứu sốc phản vệ tr−ớc khi tiêm cản quang iod .
4.3 – Các biểu hiện khác:
.Co giật; xử trí : th−ờng hết sau khi tiêm 1 ống gardenal /tĩnh mạch , hay valium 10mg/tĩnh mạch
.Cơn têtani: điều trị bằng tiêm tĩnh mạch calciclorua
Nội dung hộp thuốc cấp cứu chống sốc phản vệ
( kèm theo thông t− số 09/1999-TT-BYT ngày 04 tháng 5 năm 2003)
A- Các khoản cần thiết phải có trong hộp thuốc cấp cứu : 7 khoản
1. Adrenaline 1mg – 1ml 2 ống
2. N−ớc cất 10ml 2 ống
3. Bơm và kim tiêm vô khuẩn 10ml 2cái
1ml 2cái
4. Hydrocortison hemisuccinate 100mg hoặc methylprednisolone ( Solumedrol 40mg hoặc Depersolone 30mg) 2 ống
5. Ph−ơng tiện khử trùng Bông , băng, cồn , gạc
6. Dây garô
7. Phác đồ chống sốc phản vệ
B- Tuỳ theo điều kiện trang thiết bị và trình độ chuyên môn, các cơ sở có sử dụng thuốc cản quang iod nên có các thiết bị và thuốc nh− sau :
1. Bơm xịt sabutamol hoặc terbutaline
2. Bóng ambu và mặt nạ
17
3. Dụng cụ đặt nội khí quản
– Có thể dụng loại cản quang Iode tan trong n−ớc có ion hoặc không ion. Loại không ion (omnipaque, iopamiron, ultravist…) có −u thế rất hiếm gây phản ứng phụ nh−ng giá thành cao. Loại có ion (Télébrix, Urografin, Diatriazoate…) giá thấp hơn nh−ng gây phản ứng phụ nhiều hơn nên có khi làm gián đoạn khám xét . Tỷ lệ ng−ời bệnh phải tiêm thuốc cản quang trong chụp cắt lớp rất cao, vì vậy nên chọn thuốc cản quang một cách có cân nhắc; có thể dùng loại chứa ion cho ng−ời lớn, thể trạng tốt và không nghi ngờ tiền sử dị ứng; loại không ion giành cho những ng−ời bệnh có nguy cơ cao phản ứng với thuốc cản quang nh− ng−ời già, trẻ em, ng−ời có bệnh gan, tim, thận, bệnh phổi gây giảm chức năng hô hấp.
– L−ợng thuốc cản quang thông dụng là 1 – 1,5ml/kg cơ thể, loại có hàm l−ợng Iode 320
– 350mg/ml, khoảng 50 – 120ml cho ng−ời lớn.
– Có ba cách đ−a thuốc cản quang vào tĩnh mạch.
+ Truyền tĩnh mạch nhanh dung dịch thuốc cản quang pha loãng với một l−ợng t−ơng đ−ơng n−ớc cất hoặc glucoza đẳng tr−ơng; kiểu này đ−ợc −a chuộng với các máy chụp cắt lớp quy −ớc thông dụng vì thời gian khám xét t−ơng đối kéo dài nh−ng đậm độ chất cản quan trong máu bị hạn chế, hiện không dùng vì cho chất l−ợng chẩn đoán thấp.
+ Bơm tĩnh mạch hai thì: kiểu bolus (2-3ml/s) nửa liều thuốc, phần còn lại bơm chậm (1ml/s) và bắt đầu chụp cắt lớp vào thời điểm thuốc cản quang có mặt ở phần cơ thể cần khám xét (dự đoán theo thời gian tuần hoàn). Kiểu này thích hợp với các máy quét nhanh, quét xoắn ốc và cho đậm độ cản quang trong máu cao hơn cách (1).
+ Bơm toàn bộ l−ợng thuốc cần thiết kiểu bolus và bắt đầu cắt lớp tính theo thời gian tuần hoàn. Kiểu tiêm này hay dùng cho các khám xét có kết hợp nghiên cứu động học thuốc cản quang (dynamic scanning) của ổ bệnh.
Bảng thời gian tuần hoàn (tham khảo) tính từ thời điểm bắt đầu bơm thuốc ở tĩnh mạch nền cánh tay cho tới một số tạng cần khám xét theo N. Schad với tần số tim 75 lần/phút.
Cánh tay – Thất phải 4 sec
Cánh tay – Thất trái 11 sec
Cánh tay – Động mạch chủ ngực 12 sec
Cánh tay – Động mạch chủ bụng 13 sec
Cánh tay – Động mạch chậu 15 sec
Cánh tay – Não 13 sec
– Thuốc cản quang uống.
– Có thể dùng chất cản quang Iode hoà loãng hoặc Bari Suynfat hoà loãng nh−ng Iode đ−ợc −a chuộng hơn nhiều vì không xảy ra lắng đọng tạo ra hiện t−ợng cản quang không đồng nhất.
– Những ng−ời bệnh nghi ngờ có thủng ống tiêu hoá hoặc chuẩn bị phẫu thuật tiêu hoá không đ−ợc cho uống bari suynfat.
– Thuốc cản quang iode th−ờng gây tăng nhu động ruột, đôi khi có thể gây ỉa chảy nh−ng sẽ tự khỏi sau khi tháo hết thuốc.
– Để đạt đ−ợc dung dịch có đậm độ 150 – 200 đơn vị Hounsfield (HU) có thể pha loãng 3ml thuốc cản quang ionic có hàm l−ợng Iode 370mg/ml với 100ml dung dịch Manitol 4% hoặc Sorbitol 4%. Lí do sử dụng Manitol hoặc Sorbitol là tạo cho dung dịch uống không còn vị đắng của thuốc cản quang và làm cho áp suất thẩm thấu của dung dịch gần với áp suất thẩm thấu của huyết t−ơng, do đó tránh đ−ợc hiện t−ợng cô đặc thuốc cản quang trong ống tiêu hoá khi pha bằng n−ớc đơn thuần.
– Ngoài ra, n−ớc tinh khiết cũng có thể dùng nh− một chất đối quang âm tính trong ống tiêu hoá.
18
– Có ba kiểu sử dụng thuốc cản quang ống tiêu hoá là. + Tạo đối quang vùng bụng trên:
Cho ng−ời bệnh uống 400ml dung dịch cản quang ngay tr−ớc khám xét tuỵ tạng, th−ợng thận v.v…
Để khám dạ dày cần cho uống 500 – 600ml để dạ dày giãn đạt mức có thể đánh giá đúng độ dầy của thành dạ dầy.
+ Tạo đối quang toàn bộ ống tiêu hoá: L−ợng thuốc cần thiết từ 1200 – 1500ml, bắt đầu cho uống 60 phút tr−ớc khám xét chia làm nhiều lần uống cách nhau 10 phút; uống lần cuối cùng ngay tr−ớc lúc ng−ời bệnh lên bàn khám xét.
+ Tạo đối quang trực tràng – Sigma trong khám xét tiểu khung: Bơm qua ống thông hậu môn 250ml dung dịch cản quang nói trên ngay tr−ớc thời điểm chụp cắt lớp. Có tác giả còn bơm thêm 50ml không khí sau khi bơm thuốc cản quang để tạo hình đối quang kép ở trực tràng.
– Đặt tăm-pông âm đạo: Dùng vài mảnh gạc vô trùng đặt vào âm đạo tr−ớc khi khám xét vùng tiểu khung của ng−ời bệnh nữ cho phép dễ nhận biết mối t−ơng quan cơ thể học bàng quang – âm đạo – trực tràng trên các lớp cắt.
– Chụp cắt lớp vi tính cho từng phần cơ thể phải làm theo những kỹ thuật riêng biệt nên phần này sẽ đ−ợc trình bầy d−ới đây theo vùng giải phẫu .


trị số hấp thụ QTX là gì ạ, mà hình 1a 1b e không thấy ạ, chỗ phần nguyên lý tạo ảnh.